ここから本文です
腸内に共生する肺炎桿菌の肝臓への感染拡大戦略の解明と肝臓がんとの関連性の発見 ~肺炎桿菌感染症の予防法及び肝臓がんの新規バイオマーカーや治療法開発に向けて新しい概念を提示~
2026年03月31日
■研究概要
腸内細菌は、がん、代謝疾患、免疫疾患などあらゆる全身性疾患の発症要因となり、治療応答性にも影響することが明らかになりはじめ、腸内細菌を軸とする遠隔臓器間ネットワークが生体の恒常性に強く貢献していると考えられています。しかし、このような臓器間ネットワークがどのように形成されているのかはほとんど理解されておらず、腸内細菌を標的とした疾患予防・治療介入法の開発研究も十分に進んでいません。
津川仁准教授(東海大学医学部生体防御学領域)と松﨑潤太郎教授(慶應義塾大学薬学部創薬研究センター)などの共同研究チームは、腸内細菌のKlebsiella pneumoniae(肺炎桿(かん)菌(きん))*1が分泌する細胞外小胞*2(Klebsiella pneumoniae -derived extracellular vesicles, KpEVs)が消化管から肝臓へ移行し、マクロファージ*3の表現型を"異物排除能が消失した炎症性免疫抑制型"に改変し、本菌の肝臓への感染を招くとともに、肝臓がんとも関連することを見出しました。つまり、KpEVsは肺炎桿菌の遠隔臓器でのコロニー形成と肝臓発がんの両方を促進する免疫抑制型の肝微小環境を形成し、肝臓がんおよび関連肝疾患の治療標的・診断バイオマーカーとして有望であることを明らかにしました。
|
研究のポイント ●肺炎桿菌が放出する細胞外小胞(KpEVs)はマクロファージを"炎症性M2型"に改変する。 ●KpEVsに内包されるsmall RNAはヒト血清中に存在し、肝臓がん患者でその存在量が上昇する。 ●KpEVsは肺炎桿菌の腸管から肝臓への伝播とがんの発生・進展に必要な免疫抑制型の肝微小環境を形成する。 |
この研究成果は、日本時間2026年3月26日(木)〔米国太平洋時間3月26日(木)〕公開の国際学術誌『Journal of Extracellular Vesicles』(IF:14.5)オンライン版に掲載されました。
■研究背景
Klebsiella pneumoniae(肺炎桿菌)は、土壌、水、植物など自然界にも広く分布するヒト腸内細菌の一つです。肺炎桿菌の保菌率は健常人で5~38%ですが、入院患者になるとその保菌率は著しく上昇します。肺炎桿菌が臨床的に重要となる局面は、本菌による消化管外感染症が発生する点にあります。肺炎桿菌の保菌者では非保菌者に比べて消化管外感染症の発症リスクが有意に高く、消化管外感染菌株の多くが腸管内保菌株と一致します。つまり、肺炎桿菌が消化管内から遠隔臓器へと伝播し感染を樹立することが、本菌感染症の主たる発症メカニズムであり、この過程を阻止する方法論の確立が、院内感染の予防に直結する極めて重要な課題となっています。
近年、腸内細菌ががんの発生や進展に関与することが明らかになり始めています。発がんに関わる腸内細菌の特定やがんの発生・進展過程に関わる菌対宿主の相互作用の解明は、がんの発生・進展過程の多様性の理解に貢献し、腸内細菌を標的とした革新的ながん予防・治療法の開発に繋がると期待されています。
■研究成果
(1) 肝臓がん患者の血清中で、腸内細菌由来のsmall RNA量が上昇する。
研究チームは、ヒト血清中には細菌由来のtransfer RNA(tRNA)*4の断片(transfer small RNA, tsRNA)が存在し、その存在量は健常者に比べ肝臓がん患者で顕著に増加することを見出しました(図1)。興味深いことに、このtsRNAはKpEVsに内包されており、マクロファージなどの宿主細胞内へ効率的に送達されることを明らかにしました。送達されたtsRNAは、マクロファージの一酸化窒素(NO)*5産生を阻害し、病原体排除能を低下させることを明らかにしました。マクロファージによるNO産生は、がん細胞の排除にも関わる重要ながん免疫応答のひとつでもあり、KpEVsのtsRNA送達によるNO産生の抑制はがん免疫の破綻にもつながります。本研究により、血清中tsRNAが従来の血液検査では捉えられない新しいタイプの肝臓がんバイオマーカーとなり得ることが明らかになり、肝臓がん発症リスクをより早期に評価できる新たな診断手法の開発につながると期待しています。
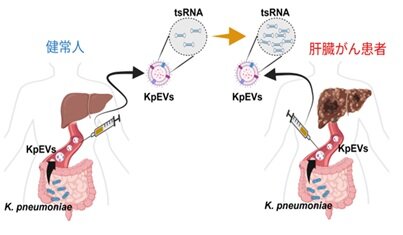
図1. 腸内細菌が分泌するKpEVsに含まれるtsRNAは肝臓がん患者でより多く検出された
(2) KpEVsは肝臓へ集積し、マクロファージを"異物排除能が失われた炎症性M2型"へ改変し肺炎桿菌の肝臓への感染拡大を導く。
研究チームは、KpEVsがマクロファージの表現型を細菌にとって都合のよい"免疫抑制状態"へと切り替えるため、肺炎桿菌はマクロファージによる排除応答を回避しマクロファージ内での生存を樹立することを明らかにしました。KpEVsはマクロファージに対して、tsRNA送達によるNO産生抑制のみならず、貪食能を亢進させたM2型*6へと誘導し、さらに、炎症性サイトカイン(IL-1β)産生を増強させるが、炎症性プログラム細胞死(パイロトーシス)は抑制することを明らかにしました(図2)。このようなKpEVsが誘導する "異物排除能が失われた炎症性M2型マクロファージ"はこれまでに類を見ないマクロファージの新しい表現型であり、研究チームはこれを"ゾンビマクロファージ"と呼称しています。KpEVsによるゾンビマクロファージの形成は、がん免疫の破綻でもありがん細胞の発生・進展過程にも有利に働くと考えられます。さらに研究チームは、消化管内のKpEVsが血中を介して肝臓に集積することを確認しました。KpEVsが蓄積した肝臓では、M2型マクロファージが増え、NOを産生するための酵素(誘導型一酸化窒素合成酵素, Inducible Nitric Oxide Synthase, iNOS*7)の発現が抑制されました。KpEVsが蓄積した肝臓では、腸管から肝臓への肺炎桿菌の伝播が顕著に増加しました。
我々研究チームは、肺炎桿菌はKpEVsを肝臓へ行かせて肝臓マクロファージをゾンビ化し、自身が肝臓への感染拡大を容易にするための微小環境を遠隔で形成することを明らかにし、この肺炎桿菌のKpEVsを利用した感染拡大戦略は肝臓がんの発生とも関連することを明らかにしました。
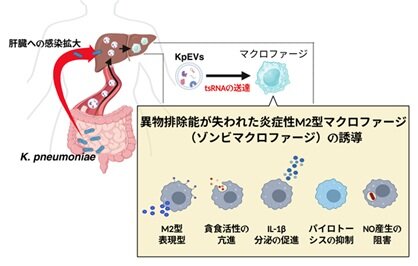
図2. KpEVsによるマクロファージの表現型の変容 (ゾンビ化)
■本研究の意義と今後の展望
研究チームは、肺炎桿菌由来の細胞外小胞(KpEVs)がマクロファージをハイジャックすることで腸と肝臓のあいだに"炎症誘導性の免疫抑制型"コミュニケーションを形成し、肺炎桿菌が肝臓への感染拡大を成功させる仕組みを解明しました。肺炎桿菌のKpEVsを用いた感染拡大戦略は肝膿瘍だけでなく肝臓がんの発生にも関与し得る腸内細菌を軸とした腸肝ネットワークとして位置づけられ、これまで見過ごされてきた腸内細菌の生体内挙動と疾患発症を具体的につなぎ合わせた重要な発見です。さらに、KpEVsに封入されるtsRNAは血液中で検出可能であり、肝臓がんリスクを捉える非侵襲的バイオマーカーとして、また、細菌が関与する発がんプロセスの指標として、その応用性が強く期待されます。「腸内細菌由来細胞外小胞を介した腸肝ネットワーク」は、がんの発生・進展における多様性を理解するうえで極めて重要な視点であり、がんの診断や予防法の開発戦略に新しい洞察を与えます。
■特記事項
本研究は次の支援をもとに行われました。東海大学医学部プロジェクト研究助成[代表:津川仁(東海大学医学部)]、東海大学医学研究基金[代表:津川仁(東海大学医学部)]、東海大学総合医学研究所コアプロジェクト2[代表:津川仁(東海大学医学部)]、シオノギ感染症研究振興財団[代表:津川仁(東海大学医学部)]、公益財団法人発酵研究所[代表:津川仁(東海大学医学部)]および、AMED《革新的がん医療実用化研究事業》『細菌由来の細胞外小胞を活用したがんリスク診断・予防法の開発』[代表:松﨑潤太郎(慶應義塾大学薬学部)]
■掲載論文
|
掲載誌 |
: |
Journal of Extracellular Vesicles |
|
タイトル |
: |
Gut commensal Klebsiella pneumoniae extracellular vesicles shape a liver microenvironment conducive to gut-liver bacterial translocation and pro-tumorigenic processes |
|
掲載日 |
: |
日本時間2026年3月26日(木)〔米国太平洋時間3月26日(木)〕 |
|
著者 |
: |
Shogo Tsubaki1, Sho Nashimoto1, Rika Tanaka2, Touya Toyomoto1, Hiroyasu Tsutsuki3, Ken Kato4, Jun Nakayama5,6, Kiminori Kimura7, Kazuki Oshima8, Yusuke Yamamoto5, Takuji Okusaka9, Minoru Esaki10, Nobuhiro Kawai11, Nobuyuki Ota11, Yusuke Yoshioka12, Takahiro Ochiya12, Yoshimasa Saito8, Tomohiro Sawa3, Katsuto Hozumi2, Juntaro Matsuzaki13, 14*, Hitoshi Tsugawa1,15*(*Corresponding Author) |
|
所属情報 |
: |
1. 東海大学医学部医学科基礎医学系生体防御学領域・生物界間シグナル解析ユニット 2. 東海大学医学部医学科基礎医学系生体防御学領域・免疫学ユニット 3. 熊本大学大学院生命科学研究部(医学系) 微生物学分野 4. 国立がん研究センター中央病院 頭頸部・食道内科/消化管内科 5. 国立がん研究センター 病態情報学ユニット 6. 大阪国際がんセンター研究所 腫瘍増殖制御学部 7. 東京都立病院機構 がん・感染症センター都立駒込病院 8. 慶應義塾大学薬学部 薬物治療学講座 9. 国立がん研究センター中央病院 肝胆膵内科 10. 国立がん研究センター中央病院 肝胆膵外科 11. Preferred Medicine 12. 東京医科大学 医学総合研究所 分子細胞治療研究部門 13. 慶應義塾大学薬学部 創薬研究センター ナノ医薬・分野横断遺伝学講座 14. 慶應義塾大学 WPI-Bio2Q 15. 東海大学総合医学研究所 |
|
DOI |
: |
10.1002/jev2.70262 |
|
URL |
: |
■用語解説
*1 Klebsiella pneumoniae(肺炎桿(かん)菌(きん)):腸内細菌科のKlebsiella属に属するグラム陰性の桿菌。非運動性で、莢膜と呼ばれる細胞壁の外側に位置する多糖類やポリペプチドから構成された被膜状構造をもつ。近年、β-ラクタマーゼやカルバペネマーゼを産生する抗菌薬耐性菌株の増加が懸念されている。
*2 細胞外小胞(Extracellular Vesicles, EVs):真核細胞・原核細胞の区別なくほぼすべての細胞から放出される脂質二重膜に包まれた微小な粒子(粒子径は約40 nm~数 百nm)で、内部にタンパク質やRNAなどの核酸を内包し、細胞間コミュニケーションや病態形成において重要な役割を果たしていると考えられています。
*3マクロファージ:全身の組織に広く分布している細胞で、体内に侵入した細菌などの異物を貪食し消化・殺菌する自然免疫機能を担う免疫細胞。
*4 transfer RNA(転移RNA, tRNA):細胞内のタンパク質合成の過程(翻訳)で、メッセンジャーRNA(mRNA)の遺伝子(コドン)に対応するアミノ酸を蛋白質合成の場(リボソーム)へ運んでくる約70〜90塩基から成るRNA分子。
*5 一酸化窒素(NO):血管の内皮細胞やマクロファージから産生される無色・無臭の生体内ガス分子。血管の弛緩・拡張を制御し、また、細菌や寄生虫などの感染防御効果も発揮する。がん細胞に対する排除応答(がん免疫)にも関わる。
*6 M2型マクロファージ:マクロファージの表現型はM1とM2に分類することができ、M2型に分類されるマクロファージは、組織修復・免疫抑制・恒常性維持を担う"治し屋"タイプの性質を示し、一方、M1型マクロファージとは、炎症誘導性の攻撃型(異物排除活性の強い)タイプの性質を示すマクロファージのことをいう。
*7 誘導型一酸化窒素合成酵素(Inducible Nitric Oxide Synthase, iNOS):マクロファージをはじめとする免疫細胞が異物を認識し「戦闘モード」に入ったときに大量の一酸化窒素(NO)を作り出すための酵素。
|
<研究に関するお問い合わせ> 東海大学医学部医学科基礎医学系生体防御学 東海大学総合医学研究所 津川 仁 TEL. 0463-93-1121(代表)
<本件に関するお問い合わせ> 東海大学医学部付属病院事務部事務課(広報) 後藤・藤岡・山口 TEL.0463-90-2001(直通) E-mail:prtokai@tokai.ac.jp
慶應義塾広報室 宮崎 TEL.03-5427-1541(直通) E-mail:m-pr@adst.keio.ac.jp |

