ここから本文です
アフラトキシンの産生制御メカニズムを解明カビのアフラトキシン産生はミトコンドリア代謝により調節される
2020年09月09日
帝京大学理工学部バイオサイエンス学科教授 作田庄平、同博士研究員 古川智宏(現 国立研究開発法人 農業・食品産業技術総合研究機構)、東海大学工学部生命化学科准教授 片山秀和氏、東京大学大学院農学生命科学研究科教授 高山誠司氏、同准教授 鈴木道生氏、山形大学農学部食料生命環境学科教授 及川彰氏らの共同研究グループは、アフラトキシン産生を阻害する物質として見出していたジオクタチンが、ミトコンドリアのプロテアーゼに結合してこれを異常に活性化し、ミトコンドリア内のエネルギー産生関連タンパク質の過剰な分解を引き起こすことにより、アフラトキシン産生の減少を招くことを発見しました。アフラトキシンは、カビが感染した食品中に産生される、強力な発がん性を持つカビ毒です。現在、肝臓がんの三分の一はアフラトキシンが原因で発症し、50億人がアフラトキシン汚染による健康被害リスクにさらされています。また、アフラトキシン汚染食品の破棄は、甚大な経済被害をもたらしています。アフラトキシン汚染の効果的な防除方法の開発は喫緊の課題ですが、そのためにはカビの持つアフラトキシン産生制御メカニズムの解明が必要です。この結果は、カビの二次代謝産物であるアフラトキシン産生がミトコンドリアの代謝機能によりコントロールされていることを示しており、食品のアフラトキシン汚染防除法の開発に資する新たな知見を提供するものです。
本研究の成果は、2020年9月3日付で米国科学雑誌「Cell Chemical Biology」に掲載されました。
【ポイント】
■アフラトキシンの産生制御メカニズムの解明は、アフラトキシン汚染防除法を開発するために重要であるが、二次代謝産物であるアフラトキシンの一次代謝での産生制御メカニズムはこれまで不明であった。今回、ミトコンドリアの代謝機能によりアフラトキシン産生が制御されていることをはじめて示した。
■アフラトキシン産生制御メカニズムを解明するために、アフラトキシン産生阻害物質であるジオクタチンの作用メカニズムを解析し、ジオクタチンはミトコンドリア内のClpプロテアーゼに結合しこれを活性化することを明らかにした。
■ジオクタチンにより活性化されたClpプロテアーゼは、ミトコンドリアのエネルギー産生関連タンパク質を選択的に分解することを発見した。
■ジオクタチンにより解糖系とアルコール発酵にかかわる遺伝子発現および中間物質が増加し、ヒストン修飾が変化してアフラトキシン生合成遺伝子群の発現が抑制されることを明らかにした。
【研究背景と内容】
アフラトキシンは、Aspergillus flavusなどの一部のAspergillus属真菌が産生する強力な発がん性物質です。熱帯・亜熱帯地域において、アフラトキシン産生菌が感染したトウモロコシやピーナッツなどの農産物にアフラトキシンが蓄積され、これを摂取したヒトや家畜に中毒症状を引き起こすとともに、汚染農産物の廃棄に伴う甚大な経済被害をもたらしています。汚染農作物からアフラトキシンを除去することは難しく、また、通常の調理方法では分解されない熱安定性を持つため、農産物のアフラトキシン汚染自体を防除する必要があります。しかし、現状では有効な防除方法はほとんどありません。効果的な防除方法の開発には、真菌のアフラトキシン産生制御メカニズムの解明が必要です。真菌は、自身の成育には必要なく、産生にどのような生理的意義があるのかわからない化合物を二次代謝で数多く産生します。そのような二次代謝産物には、特異な生物活性を持つ化合物が多く含まれ、アフラトキシンも二次代謝産物の一つです。二次代謝に対して、成育に必須である代謝を一次代謝と呼びますが、一次代謝から二次代謝に移行する際の調節メカニズムはほとんどわかっていません。作田教授らのグループは、アフラトキシン産生を特異的に阻害する活性物質に着目し、その作用メカニズムの解析を糸口として、一次代謝でのアフラトキシン産生制御メカニズムを調べてきました。
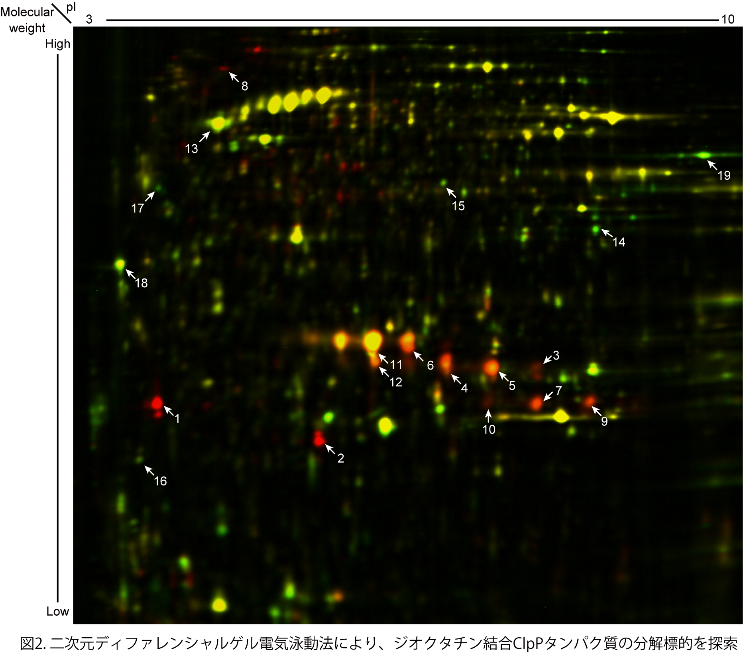
本研究では、強いアフラトキシン産生阻害活性を見出していましたが、その作用メカニズムは未解明であった物質ジオクタチンについて解析しました。まず、有機合成によりジオクタチン分子を固定化したナノ磁気担体を調製しジオクタチン結合タンパク質の精製を試みたところ (図1)、ミトコンドリア内のプロテアーゼであるClpプロテアーゼ (ClpP) が同定されました。通常、ClpPはシャペロンタンパク質と複合体を形成し、シャペロンなしでは基質となるタンパク質を分解できません。しかし、精製したClpPタンパク質を用いた実験の結果、ジオクタチンの存在下ではClpPはシャペロンなしで基質タンパク質を分解できることが見出されました。そこで、ジオクタチンにより活性化されたClpPタンパク質がミトコンドリア内のタンパク質を分解するかどうか、その場合は標的となるタンパク質に選択性があるかどうかを、特殊な電気泳動法により調べました(図2)。 結果として、ジオクタチン結合ClpPはミトコンドリアの呼吸鎖複合体など、エネルギー代謝に関係するタンパク質を選択的に分解することがわかりました。ClpPの遺伝子破壊した変異体では、ジオクタチンを添加しても呼吸鎖複合体の減少は見られなかったことから、ジオクタチン結合ClpPは細胞内において、確かに代謝関連タンパク質分解を引き起こしていると考えられました。さらに、真菌細胞内の全代謝物質変動解析と、遺伝子発現変動解析を行ったところ、ジオクタチンによってアフラトキシン生合成に関与する遺伝子群の発現が抑制されることが確認されるとともに、ミトコンドリアクエン酸回路の物質が減少する一方、解糖系の中間物質とアルコール発酵経路の物質、およびこれらの経路に関与する酵素の遺伝子発現が増加することが示され、ジオクタチンにより細胞内のエネルギー産生がミトコンドリアから解糖系およびアルコール発酵にシフトしていることが推察されました。最後に、アフラトキシン生合成酵素遺伝子の発現との相関が報告されているヒストンタンパク質の修飾を調べたところ、ジオクタチンによりアセチル化修飾が減少することがわかりました。
以上から、ジオクタチンによるClpプロテアーゼの異常活性化によりミトコンドリアのエネルギー産生関連タンパク質が分解され、エネルギー産生が解糖系にシフトするとともにヒストン修飾が変化し、アフラトキシン生産関連遺伝子の発現減少とアフラトキシン産生の抑制が起こると考えられました。本研究の結果は、二次代謝産物であるアフラトキシンの産生が、一次代謝であるミトコンドリアの代謝機能により制御されていることを示しています。
【成果の意義】
アフラトキシン汚染問題は、人類にとって解決が急がれる課題です。温暖化が進み、アフラトキシン汚染が生じる地域が拡大しており、日本においても近い将来、問題となる汚染が生じる可能性が十分にあります。アフラトキシンを産生するAspergillus属真菌は、抗カビ剤に対する耐性が高く、圃場で使用できる抗カビ剤は現在開発されていません。抗カビ剤の使用は、耐性菌の問題もあります。そこで、二次代謝産物であるアフラトキシンの産生だけを選択的に抑制してアフラトキシン汚染を防除する方法が考えられます。本研究で明らかにした、ミトコンドリアの代謝機能によるアフラトキシン産生制御メカニズムは、より標的特異的なアフラトキシン汚染防除法の開発に貢献することが期待されます。また、現在不明である、他の真菌の二次代謝調節メカニズムを解明する研究の端緒になると考えられます。
【論文情報】
雑誌名: Cell Chemical Biology (9月3日オンライン公開)
論文タイトル: Dioctatin activates ClpP to degrade mitochondrial components and inhibits aflatoxin production
著者: Tomohiro Furukawa, Hidekazu Katayama, Akira Oikawa, Lumi Negishi, Takuma Ichikawa, Michio Suzuki, Kohji Murase, Seiji Takayama and Shohei Sakuda* (*責任著者)
DOI番号: https://doi.org/10.1016/j.chembiol.2020.08.006
論文URL: https://www.cell.com/cell-chemical-biology/fulltext/S2451-9456(20)30303-2
【著者所属】
帝京大学理工学部バイオサイエンス学科(作田庄平、古川智宏*)
(*現所属:国立研究開発法人 農業・食品産業技術総合研究機構)
東海大学工学部生命化学科(片山秀和 市川琢万)
東京大学定量生命科学研究所(根岸瑠美)
東京大学大学院農学生命科学研究科(鈴木道生、村瀬浩司、高山誠司)
山形大学農学部食料生命環境学科(及川彰)
【研究費】
・農林水産省委託プロジェクト研究 (13406478-4)
・科学研究費助成事業 (19K15760)
■本件に関するお問い合わせ
東海大学 大学広報部企画広報課
TEL:0463-50-2402 FAX:0463-50-2215
E-mail:pr@tsc.u-tokai.ac.jp
本研究の成果は、2020年9月3日付で米国科学雑誌「Cell Chemical Biology」に掲載されました。
【ポイント】
■アフラトキシンの産生制御メカニズムの解明は、アフラトキシン汚染防除法を開発するために重要であるが、二次代謝産物であるアフラトキシンの一次代謝での産生制御メカニズムはこれまで不明であった。今回、ミトコンドリアの代謝機能によりアフラトキシン産生が制御されていることをはじめて示した。
■アフラトキシン産生制御メカニズムを解明するために、アフラトキシン産生阻害物質であるジオクタチンの作用メカニズムを解析し、ジオクタチンはミトコンドリア内のClpプロテアーゼに結合しこれを活性化することを明らかにした。
■ジオクタチンにより活性化されたClpプロテアーゼは、ミトコンドリアのエネルギー産生関連タンパク質を選択的に分解することを発見した。
■ジオクタチンにより解糖系とアルコール発酵にかかわる遺伝子発現および中間物質が増加し、ヒストン修飾が変化してアフラトキシン生合成遺伝子群の発現が抑制されることを明らかにした。
【研究背景と内容】
アフラトキシンは、Aspergillus flavusなどの一部のAspergillus属真菌が産生する強力な発がん性物質です。熱帯・亜熱帯地域において、アフラトキシン産生菌が感染したトウモロコシやピーナッツなどの農産物にアフラトキシンが蓄積され、これを摂取したヒトや家畜に中毒症状を引き起こすとともに、汚染農産物の廃棄に伴う甚大な経済被害をもたらしています。汚染農作物からアフラトキシンを除去することは難しく、また、通常の調理方法では分解されない熱安定性を持つため、農産物のアフラトキシン汚染自体を防除する必要があります。しかし、現状では有効な防除方法はほとんどありません。効果的な防除方法の開発には、真菌のアフラトキシン産生制御メカニズムの解明が必要です。真菌は、自身の成育には必要なく、産生にどのような生理的意義があるのかわからない化合物を二次代謝で数多く産生します。そのような二次代謝産物には、特異な生物活性を持つ化合物が多く含まれ、アフラトキシンも二次代謝産物の一つです。二次代謝に対して、成育に必須である代謝を一次代謝と呼びますが、一次代謝から二次代謝に移行する際の調節メカニズムはほとんどわかっていません。作田教授らのグループは、アフラトキシン産生を特異的に阻害する活性物質に着目し、その作用メカニズムの解析を糸口として、一次代謝でのアフラトキシン産生制御メカニズムを調べてきました。
本研究では、強いアフラトキシン産生阻害活性を見出していましたが、その作用メカニズムは未解明であった物質ジオクタチンについて解析しました。まず、有機合成によりジオクタチン分子を固定化したナノ磁気担体を調製しジオクタチン結合タンパク質の精製を試みたところ (図1)、ミトコンドリア内のプロテアーゼであるClpプロテアーゼ (ClpP) が同定されました。通常、ClpPはシャペロンタンパク質と複合体を形成し、シャペロンなしでは基質となるタンパク質を分解できません。しかし、精製したClpPタンパク質を用いた実験の結果、ジオクタチンの存在下ではClpPはシャペロンなしで基質タンパク質を分解できることが見出されました。そこで、ジオクタチンにより活性化されたClpPタンパク質がミトコンドリア内のタンパク質を分解するかどうか、その場合は標的となるタンパク質に選択性があるかどうかを、特殊な電気泳動法により調べました(図2)。 結果として、ジオクタチン結合ClpPはミトコンドリアの呼吸鎖複合体など、エネルギー代謝に関係するタンパク質を選択的に分解することがわかりました。ClpPの遺伝子破壊した変異体では、ジオクタチンを添加しても呼吸鎖複合体の減少は見られなかったことから、ジオクタチン結合ClpPは細胞内において、確かに代謝関連タンパク質分解を引き起こしていると考えられました。さらに、真菌細胞内の全代謝物質変動解析と、遺伝子発現変動解析を行ったところ、ジオクタチンによってアフラトキシン生合成に関与する遺伝子群の発現が抑制されることが確認されるとともに、ミトコンドリアクエン酸回路の物質が減少する一方、解糖系の中間物質とアルコール発酵経路の物質、およびこれらの経路に関与する酵素の遺伝子発現が増加することが示され、ジオクタチンにより細胞内のエネルギー産生がミトコンドリアから解糖系およびアルコール発酵にシフトしていることが推察されました。最後に、アフラトキシン生合成酵素遺伝子の発現との相関が報告されているヒストンタンパク質の修飾を調べたところ、ジオクタチンによりアセチル化修飾が減少することがわかりました。
以上から、ジオクタチンによるClpプロテアーゼの異常活性化によりミトコンドリアのエネルギー産生関連タンパク質が分解され、エネルギー産生が解糖系にシフトするとともにヒストン修飾が変化し、アフラトキシン生産関連遺伝子の発現減少とアフラトキシン産生の抑制が起こると考えられました。本研究の結果は、二次代謝産物であるアフラトキシンの産生が、一次代謝であるミトコンドリアの代謝機能により制御されていることを示しています。
【成果の意義】
アフラトキシン汚染問題は、人類にとって解決が急がれる課題です。温暖化が進み、アフラトキシン汚染が生じる地域が拡大しており、日本においても近い将来、問題となる汚染が生じる可能性が十分にあります。アフラトキシンを産生するAspergillus属真菌は、抗カビ剤に対する耐性が高く、圃場で使用できる抗カビ剤は現在開発されていません。抗カビ剤の使用は、耐性菌の問題もあります。そこで、二次代謝産物であるアフラトキシンの産生だけを選択的に抑制してアフラトキシン汚染を防除する方法が考えられます。本研究で明らかにした、ミトコンドリアの代謝機能によるアフラトキシン産生制御メカニズムは、より標的特異的なアフラトキシン汚染防除法の開発に貢献することが期待されます。また、現在不明である、他の真菌の二次代謝調節メカニズムを解明する研究の端緒になると考えられます。
【論文情報】
雑誌名: Cell Chemical Biology (9月3日オンライン公開)
論文タイトル: Dioctatin activates ClpP to degrade mitochondrial components and inhibits aflatoxin production
著者: Tomohiro Furukawa, Hidekazu Katayama, Akira Oikawa, Lumi Negishi, Takuma Ichikawa, Michio Suzuki, Kohji Murase, Seiji Takayama and Shohei Sakuda* (*責任著者)
DOI番号: https://doi.org/10.1016/j.chembiol.2020.08.006
論文URL: https://www.cell.com/cell-chemical-biology/fulltext/S2451-9456(20)30303-2
【著者所属】
帝京大学理工学部バイオサイエンス学科(作田庄平、古川智宏*)
(*現所属:国立研究開発法人 農業・食品産業技術総合研究機構)
東海大学工学部生命化学科(片山秀和 市川琢万)
東京大学定量生命科学研究所(根岸瑠美)
東京大学大学院農学生命科学研究科(鈴木道生、村瀬浩司、高山誠司)
山形大学農学部食料生命環境学科(及川彰)
【研究費】
・農林水産省委託プロジェクト研究 (13406478-4)
・科学研究費助成事業 (19K15760)
■本件に関するお問い合わせ
東海大学 大学広報部企画広報課
TEL:0463-50-2402 FAX:0463-50-2215
E-mail:pr@tsc.u-tokai.ac.jp