ここから本文です
100人に1人の自閉スペクトラム症 原因は「胎児期の細胞分化の乱れ」 ~脳発達の鍵「Notchシグナル」の異常を解明 新たな出生前医療の可能性を提示~
2026年03月27日
東海大学[伊勢原キャンパス]医学部の飯島 崇利 准教授と理化学研究所脳神経科学研究センターの半野 陽子 研究員を中心とする研究グループは、神戸大学大学院医学研究科の内匠 透 特命教授らとの共同研究により、複数の自閉スペクトラム症(ASD)モデルに共通する分子病態として、胎生期の脳における「Notch(ノッチ)シグナル伝達系」*1の過剰な活性化を発見し、この異常が特定の神経細胞(VIP陽性抑制性神経細胞*2)への分化を妨げ、社会性障害などの中核症状を引き起こすことを解明しました。
さらに、胎生期のマウスにNotch活性阻害剤を投与することで、成長後のASD様行動が劇的に改善することを確認しました 。本成果は、一生涯完治しないとされてきたASDの中核症状に対し、「胎生期・発達期を標的とした新たな治療戦略」という画期的な道筋を示すものです。
研究のポイント
| ● | 共通病態の発見 | : | 多様な要因を持つASDモデルにおいて、胎生脳での「Notchシグナル」の過剰活性化が共通の病態であることを同定。 |
| ● | 分化異常の解明 | : | Notchの活性亢進が、高次脳機能に不可欠な「VIP陽性抑制性神経細胞(VIP-INs)」への分化を選択的に抑制し、回路障害を誘導することを発見。 |
| ● | 症状の劇的改善 | : | 胎生期のNotchシグナルを阻害(遺伝学的および薬理学的)することで、成長後の社会性行動異常や常同行動が改善することを証明。 |
| ● | 新たな治療パラダイム | : | 「胎生期」という脳発達の根源的な時期への介入が、ASDの根本的な治療戦略となる可能性を提示 。 |
この研究成果は、日本時間2026年3月30日(月)18:00(日本時間)公開の国際学術誌『Nature Communications』オンライン版に掲載されます。
■研究背景:ASDの普遍的な発症原理を求めて
自閉スペクトラム症(ASD)は、「社会的コミュニケーションの障害」と「行動や興味の偏り」という二つの中核症状を示す先天的な神経発達症です。近年の有病者は100人のうち1〜3人と報告されており、幼少期に顕在化した後は基本的に一生涯完治することはないとされています 。
発症には1,200以上の関連遺伝子に加え、母胎の感染や薬剤曝露などの環境要因、さらにそれらが誘起するエピゲノム変化*3が複雑に関与しています。しかし、要因が多岐にわたる一方で、症状が2〜3歳頃から明白になることから、「胎児期から新生児期にかけての脳発達の変容」に共通の根源があると考えられてきました。この普遍的な発症原理を突き止めることが、中核症状に対する根本的な治療法を確立する上での最大の課題となっていました。
■研究成果:Notchシグナルの異常活性化が脳の細胞構成を変える
研究グループは、多様な要因を持つ複数のASDモデル(バルプロ酸*4曝露モデル、母体免疫活性化*5モデル、ヒトiPS細胞モデル等)を網羅的に解析し、以下の事実を明らかにしました。
1.Notchシグナルの過剰活性化が共通病態
環境要因(バルプロ酸曝露など)や遺伝的要因を模した複数のASDモデルの胎生脳において、神経細胞の運命決定を司るNotchシグナル(Notch1やHes5など)が顕著に過剰活性化していることを発見しました。【図1A】
2.VIP陽性抑制性神経細胞(VIP-INs)の分化抑制
Notchシグナルの異常な活性化により、大脳皮質の高次機能維持に不可欠なVIP-INsへの分化が特に影響され、細胞数が大幅に減少することを見出しました。【図1B】
3.胎生期の介入による行動異常の改善
遺伝学的な手法、および薬理学的な手法(γ-secretase阻害剤「Ro4929097」*6の投与)によって胎生期のNotch活性を阻害したところ、成長後のVIP-IN回路の異常が回復し、社会性行動異常や常同行動が劇的に改善しました。【図2】【図3】
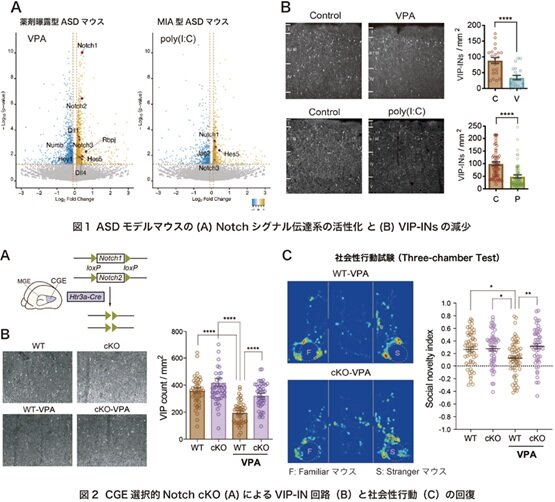
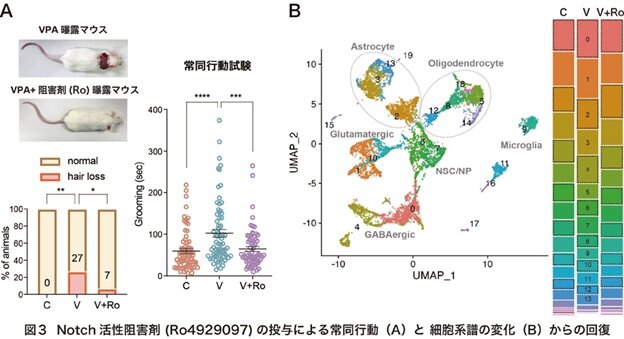
これらの結果は、胎生後期におけるNotchシグナルの異常な活性化が、ASD様行動学的表現型を引き起こす主要な分子基盤であることを示唆しています。
■今後の展望
本研究は、胎生期のNotchシグナル伝達系の調節異常がASD様症状の上流メカニズムであることを突き止めたものです。神経発達期にNotchシグナルを選択的に抑制できれば、ASDの行動障害に対する有効な治療標的となり得ることが期待されます。
今後は、より選択的な作用を持つ化合物の検討や、早期診断技術の発展と合わせることで、Notchシグナルを標的とした治療の現実を目指します。今回のモデルマウスでの成果を、ASDの中核症状に対する将来の臨床応用につなげるための第一歩としていきます。
■掲載論文
|
掲載誌 |
: |
Nature Communications |
|
タイトル |
: |
Targeting notch signaling to restore neural development and behavior in mouse models of ASD |
|
掲載日 |
: |
2026年3月30日(月)18:00〔日本時間〕 |
|
著者 |
: |
■半野 陽子 現所属:理化学研究所 脳神経科学研究センター 研究員 研究実施時所属:東海大学医学部基礎医学系 研究員 ■飯島 崇利 東海大学医学部基礎医学系生体構造学領域 准教授 ■内匠 透 神戸大学大学院医学研究科内科系講座生物学的精神医学分野 特命教授 |
|
DOI |
: |
10.1038/s41467-026-70321-6 |
|
URL |
: |
■用語解説
*1 Notchシグナル伝達系:細胞分化・増殖・運命決定を制御する重要な細胞間シグナル伝達経路です。神経発生や組織形成に深く関与します。
*2 VIP陽性抑制性神経細胞 (VIP-IN):GABAを放出する抑制性介在ニューロンの一種。脳内で神経の働きの「強さ(ゲイン)」を調節する抑制性の神経細胞です。役割の一つとして、不要なノイズを抑えながら、感覚情報を適切に伝える役割を担い、情報処理の精度を高めます。
*3エピゲノム:DNA配列を変えずに、DNAメチル化やヒストン修飾などを通じて遺伝子発現を調節する仕組みです。加齢や環境要因などさまざまな要素に影響されやすく、その変化は疾患発症に強く関与することが明らかにされてきています。
*4 バルプロ酸(VPA):抗てんかん薬や気分安定薬として使われている一般的な薬です。一方で、妊娠期に服用した場合、胎児のエピゲノムに影響を及ぼし、脳発達に悪影響を与える危険性があることが報告されています。
*5 母体免疫活性化(Maternal Immune Activation:MIA):妊娠中に母親がウイルスや細菌などに感染し、免疫反応が過剰に活性化される状態です。この影響が胎児の脳の発達に及ぶ可能性があることが知られています。
*6 γ-secretase阻害剤:Notchの活性化に関わるγ‑secretaseを阻害する薬剤です。過去にはアルツハイマー病やがん治療への応用が検討され、多くの化合物が開発されてきました。Ro4929097は、その一つです。
<研究に関するお問い合わせ>
東海大学医学部基礎医学系生体構造学領域 飯島 崇利
TEL. 0463-93-1121(代表)
理化学研究所 脳神経科学研究センター 半野 陽子
TEL. 048-462-1111(代表)
<本件に関するお問い合わせ>
東海大学医学部付属病院事務部事務課(広報) 後藤・藤岡・山口
TEL.0463-90-2001(直通) Email:prtokai@tokai.ac.jp
理化学研究所 広報部 報道担当
TEL. 050-3495-0247 Email:ex-press@ml.riken.jp

